来源:江西省药品监督管理局 时间:2023-09-05 作者:
近日,江西省发布2023年第3期药品监督抽检信息公告,公告内容具体如下:
为加强药品质量监管,保障公众用药安全,根据《中华人民共和国药品管理法》及相关法律法规和江西省药品抽检计划,我省各级药品监管部门和检验机构对全省药品生产、经营和使用单位实施了监督抽检。现将本期药品抽检信息通报如下:
一、公告情况
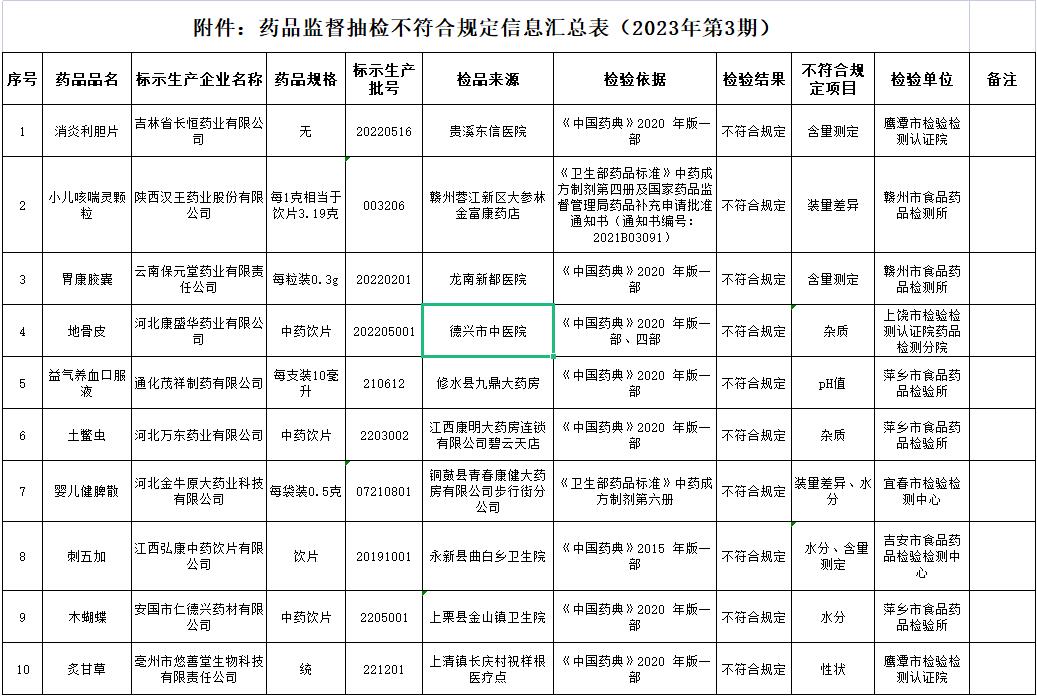
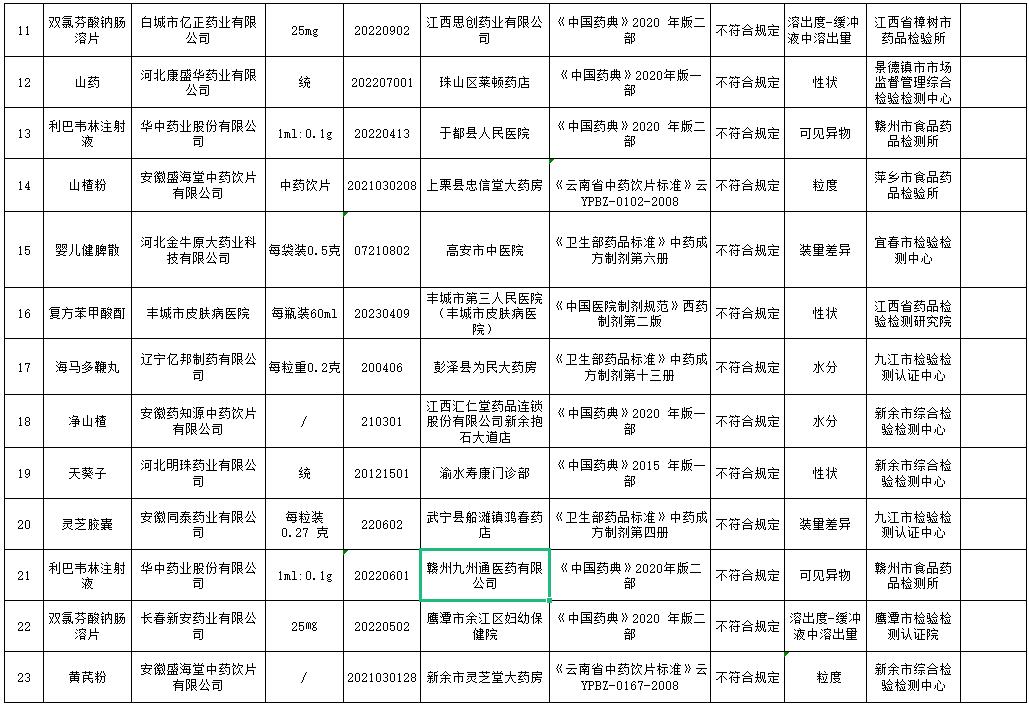
经核查确认,本期监督抽检信息公布如下:消炎利胆片等23批产品不符合规定(详见附件),不符合规定项目包括含量测定、装量差异、可见异物、性状、水分、粒度、溶出度等。
二、不符合规定药品的查处情况
江西省药品监督管理局已责成相关部门对检验不符合规定的药品采取查封、扣押、暂停销售、召回等必要的控制措施,依据相关法律法规对生产企业和被抽样单位进行查处。
附件1:药品监督抽检不符合规定信息汇总表
附件2:不符合规定项目小知识
1、性状记载产品的外观、臭、味、溶解度以及物理常数等,在一定程度上反映药品的质量特性。中药饮片性状项不符合规定,可能涉及药材种属偏差、炮制工艺有瑕疵、储存不当等情形。
2、水分是指药品中的含水量。水分偏高通常与工艺、包装不当以及储运环境等因素有关。
3、粒度是指颗粒的粗细程度及粗细颗粒的分布,用于测定药物制剂的粒子大小或限度。粒度的控制对药物的有效性、稳定性及安全性具有一定影响。
4、可见异物是指存在于注射液、眼用液体制剂和无菌原料中可目视检出的不溶性物质。
5、装量差异是药品制剂均匀性的指标之一,检查的目的在于控制单位药品装量的一致性,以确保使用剂量的准确均一。
6、含量测定是指用规定的试验方法测定原料及制剂中有效成分的含量。
7、pH值是氢离子浓度指数,作为酸碱程度的衡量指标。
8、杂质是指是指药物中存在的无治疗作用或者影响药物的稳定性、疗效,甚至对人体的健康有害的物质。
9、溶出度是指活性药物从片剂、胶囊剂或颗粒剂等普通制剂在规定条件下溶出的速率和程度,是片剂质量控制的一个重要指标。肠溶片在进行溶出度检查时,考虑为防止原料药物在胃内分解失效、对胃的刺激或控制原料药物在肠道内定位释放,一般考察酸中溶出量和缓冲液中溶出量。






